¿Cuáles son los valores del número cuántico n?
Número de teléfono cuántico principal ( n )
Numéricamente, n puede tomar valores enteros desde 1 cara arriba, o bien sea, 1, 2, 3, 4, etc. El número cuántico principal se correlaciona también con la separa promedio que existe a caballo entre el núcleo y un electrón.
Numéricamente, n puede tomar valores enteros desde 1 cara arriba, o bien sea, 1, 2, 3, 4, etc. El número cuántico principal se correlaciona también con la separa promedio que existe a caballo entre el núcleo y un electrón.
¿Qué valores puede tomar la L?
l: Número cuántico secundario o bien azimutal. Bebe valores desde 0 hasta (n-1). Nos indica la forma y el tipo del orbital.
¿Que nos indica el número cuántico l?
II) El número cuántico del instante angular ( l ), indica la constituye de los orbitales y el subnivel de energía en el que se halla el electrón, (‘ l = 0,1,2,3,4,5,…,n-1).’
¿Qué indica el número cuántico principal n?
El número cuántico principal nos indica en que nivel se encuentra el electrón, este valor estimado bebe valores enteros del 1 al 7.
- ¿Qué indica el número cuántico l?:
– El número cuántico secundario, (l) también llamado númerocuántico azimutal o número cuántico por el momento angular. halla el electrón, mientras mayor sea el valor estimado de n, más alejado esta el electrón del núcleo, y mayor es su contenido energético.
¿Qué valores tiene el número cuántico l?
II) El número cuántico secundario es L ( l = 0,1,2,3,4,5,…,n-1), indica la constituye de los orbitales y el subnivel de energía en el que se halla el electrón. Un orbital de un átomo hidrogenoide tiene l nodos angulares y n-1- l nodos radiales.
¿Qué valores puede poseer el número cuántico m?
número cuántico imantado (+)
Se escenifica por la letra m, Puede tomar cualquier valor entero comprendido a caballo entre -l y +l, siendo l el número cuántico secundario; estos 2l+1 valores posibles definen el número de orbitales atómicos de cada subcapa electrónica.
Se escenifica por la letra m, Puede tomar cualquier valor entero comprendido a caballo entre -l y +l, siendo l el número cuántico secundario; estos 2l+1 valores posibles definen el número de orbitales atómicos de cada subcapa electrónica.
¿Qué valores toma M para l?
| Evalúes permitidos | |
|---|---|
| para n: | números enteros 1, 2, 3,. |
| para l : | números enteros a cuartear de 0 hasta (n-1) |
| para m : | todos y cada uno de los números enteros entre +l y – l incluido el 0 |
| para s: | solo los números fraccionarios -1/2 y +1/2 |
¿Cuándo n 4 los valores del l están pudiendo ser?
Asimismo es notorio como el número cuántico del instante angular orbital o número cuántico azimutal y se simboliza como !13 ( L minúscula). si n = 2 ; !13 = 0, 1. si n = 4 ; !13 = 0, 1, 2, 3.
¿Cuál es el valor estimado de L en cuanto n 3?
En cuanto n = 3, l adquiere tres valores: 0, 1 y 2.. para cada valor estimado de l, y a cada orbital se le asigna una textual.
¿Qué es lo que significa la letra L en química?
L; en química y en fisica, el símbolo de la incesante de Avogadro. L ; en bioquímica, representación del aminoácido leucina.
¿Qué es el nivel de energía n?
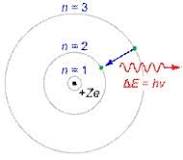
Estos niveles se designan con la letra n, adonde n es un número entero positivo. De ésta forma, n = 1 corresponde al nivel energético principal más bajo. A medida que n aumenta, también se acrecienta la energía del electrón y, en promedio, el electrón se encuentra más distanciado del núcleo.
¿Qué escenifica el primer número cuántico?
– Número cuántico principal (n)
Especifica el nivel energético del orbital, siendo el primer nivel el de menor energía, y se relaciona con la distancia promedio que hay del electrón al núcleo en un determinado orbital.
Especifica el nivel energético del orbital, siendo el primer nivel el de menor energía, y se relaciona con la distancia promedio que hay del electrón al núcleo en un determinado orbital.


















