¿Qué es un soluto volátil ejemplos?
Conocida como
Colas, lacas, quita-grasas, gasolina, pinturas, desodorizantes en spray, aromatizantes del hogar, sprays anestésicos, gas líquido, disolventes, etc.
Colas, lacas, quita-grasas, gasolina, pinturas, desodorizantes en spray, aromatizantes del hogar, sprays anestésicos, gas líquido, disolventes, etc.
- ¿Qué es un soluto volátil?:
El soluto puede llegar a ser volátil, esto es, posee una presión de vapor mayor que el 1% de la presión de vapor del solvente a la misma temperatura ; o bien no volátil, o sea, posee una presión de vapor menor de edad que el 1% de la presión de vapor del solvente a la misma temperatura.
- ¿Qué es un soluto no volatil ejemplos?:
Determinados solutos no volatiles son el azúcar, la sal, una sopa el polvo, determinados condimentos como la pimienta. Los solutos no volatiles son aquellos que no huyen, en forma de vapor, de una mezcla.
- ¿Qué es un soluto no volátil?:
El soluto puede llegar a ser volátil, o sea, tiene una presión de vapor mayor que el 1% de la presión de vapor del solvente a exactamente la misma temperatura; o no volátil, es decir, posee una presión de vapor menor que el 1% de la presión de vapor del solvente a la misma temperatura.
¿Cuándo se agrega un soluto no volátil?
En cuanto se agrega un soluto no volátil a un solvente puro, el punto de ebullición de éste aumenta. Sin duda, el punto de ebullición de un líquido ocurre en cuanto la presión de vapor de este mismo se iguala a la presión atmosférica.
- ¿Cuándo se agrega un soluto no volátil a un solvente volátil su temperatura de ebullición?:
Las propiedades coligativas apuntan que al incorporar un soluto no volátil la presión de vapor reduce, la temperatura de ebullición aumenta, el punto de congelación reduce y la presión osmótica aumenta.
- ¿Cuándo se agrega un soluto no volátil a un solvente puro la presión de vapor de esté en la solución reduce?:
Descenso de la presión de vapor
En cuanto a un solvente se le agrega un soluto no volátil, la presión de vapor del solvente tiende a descender. Este fenómeno se tiene que, eminentemente, a que el número de moléculas del solvente en la superficie libre de la solución reducen por la presencia del soluto no volátil. - ¿Cuándo se agrega un soluto no volátil a un solvente la presión de vapor de la solución?:
Si el soluto que se agrega es no volátil, se generará un descenso de la presión de vapor, puesto que este disminuye la capacidad del disolvente a pasar de la fase líquida a la fase vapor. El grado en que un soluto no volátil disminuye la presión de vapor es proporcional a su concentración.
¿Cuándo se adiciona un soluto no volátil a un solvente volátil la presión de vapor de la solución resultante con relación a la presión de vapor del solvente puro es?
En cuanto a un solvente se le agrega un soluto no volátil, la presión de vapor del solvente tiende a descender. Este mismo fenómeno se tiene que, principalmente, a que el número de moléculas del solvente en la superfície libre de la solución reducen por la presencia del soluto no volátil.
¿Qué es un solvente puro?
El solvente puro alcanza su punto de ebullición a una presión y temperatura determinada, la disolución debe usar mayor energía para llegar hasta su punto de ebullición, contrariamente a lo que está sucediendo con sus puntos de congelación, de ésto se concluye que a mayor adición de soluto a la solución, mayor sera su punto
- ¿Qué es un disolvente puro?:
Un disolvente o bien solvente es una substancia química en la cual se disuelve un soluto (un sólido, líquido o gas químicamente distinto), resultando en una sola disolución; por norma general el solvente es el componente de una disolución presente en mayor cantidad total.
¿Qué son volátiles ejemplos?
Colas, lacas, quita-grasas, gasolina, pinturas, desodorizantes en aerosol, aromatizantes del hogar, aerosoles anestésicos, gas líquido, disolventes, etc. Son substancias químicas altamente tóxicas de uso industrial y doméstico que al ser aspiradas pueden infligir graves consecuencias físicas y psíquicas.
¿Cuáles son las substancias volátiles?
Los compuestos orgánicos volátiles (COV) son todos aquellos hidrocarburos que se presentan en estado gaseoso a la temperatura entorno normal o que son muy volátiles a dicha temperatura.
¿Qué sucede cuando se agrega un soluto no volatil?
En cuanto se agrega un soluto no volátil a un solvente puro, la temperatura de congelación de este mismo disminuye. Este mismo descenso («06Tc) es la diferencia entre la temperatura de congelación de una solución a una concentración impartida y el solvente puro.
¿Que nos señala la ley de Raoult?
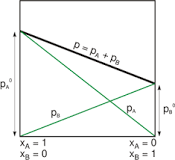
La ley de Raoult es una ley termodinámica que estipula que la presión de vapor parcial de cada componente de una mezcla idónea de líquidos es igual a la presión de vapor del componente puro multiplicado por su fracción molar en la mezcla.
¿Cuáles son las 4 propiedades coligativas?
Existen cuatro propiedades coligativas: el descenso crioscópico, el ascenso ebulloscópico, la presión osmótica y el descenso de la presión de vapor.
- ¿Que son y cuáles son las propiedades coligativas del agua?:
Resumen: Las propiedades que solo dependen de la concentración del soluto y no de la naturaleza de la molécula del solvente, son las propiedades coligativas.
¿Cuáles son las peculiaridades de las propiedades coligativas?
Las propiedades coligativas incluyen disminución de la presión de vapor, elevación de la temperatura de ebullición, descenso de la temperatura de congelación y de la presión osmótica. A partir de las propiedades coligativas se puede determinar el peso molecular de un soluto desconocido.