¿Qué importancia tiene la ley de conservacion de la masa?
¿Qué nos dice la ley de la conservación de la materia?
- ¿Que nos muestra la ley de la conservacion de la materia?:
principio de consevación de la masa o ley de Lavoisier.
La materia ni se está creando ni se destroza, solo se transforma. En una sola reacción química la suma de la masa de los reactivos es igual a la suma de la masa de los productos. En una sola reacción química los átomos no están desapareciendo, simplemente se ordenan de otra manera. - ¿Qué nos dice la ley de la conservacion de la materia?:
Ésta es la ley de la conservación de la masa, enunciándola de la siguiente manera: «En toda reacción química la masa se perpetúa, esto es, la masa total de los reactivos es igualito a la masa número total de los productos». En cuanto una candela arde no se gana ni se está perdiendo masa.
¿Qué es la ley de conservacion dela masa ejemplos?
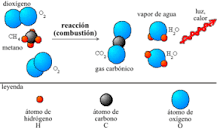
Ejemplo 1: Combustión de una candela
Cuando una candela arde no se gana ni se está perdiendo masa. La masa número total de la cera y del oxígeno molecular (O 2 ) presente antes de la combustión es igual a la masa número total de dióxido de carbono (CO 2 ), vapor de agua (H 2 O) y cera sin quemar que quedan cuando la candela se apaga.
¿Cómo es que se aplica la ley de la conservación de la materia en la vida diaria?
- La descomposición de la fruta. Es considerable la reducción del tamaño del alimento a la medida que se degrada.
- Fundir hielo. Al dejar un vasito con hielo a temperatura entorno el hielo se derrite.
- Hervir agua.
- Objetos oxidados.
- Capacitación de compuestos.
¿Cómo se manifiesta la ley de la conservación de la materia?
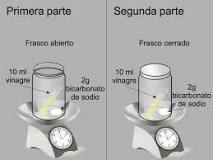
Hallazgo de la ley de conservación de la materia
Fue el científico ruso Mikhail Lomonosov (1711-1765 ) quien probó por primera vez la conservación de la materia en 1756. Lo hizo al enseñar cómo es que unas placas de plomo no cambiaban de peso mientras tanto se quemaban en un recipiente precintado (sin contacto con el aire).
- ¿Cómo es que se evidencia la ley de la conservación de la materia?:
Habia vigilado que al calentar metales como el estaño y el plomo en recipientes cerrados con una cantidad total módica de aire, éstos materiales se recubrían con una capa de carbonizado hasta un momento determinado del calentamiento, en el desenlace la masa era igual que antes de iniciar el proceso.
- ¿Cómo se demostró la ley de la conservación de la materia?:
Lavoisier demostró que al realizarse una reacción química la masa no se crea ni se destruye, sólo se transforma, es decir, las sustancias reaccionantes al interaccionar a caballo entre sí forman nuevos productos con propiedades físicas y químicas distintos a las de los reactivos, ésto dado a que los átomos de las substancias se
¿Cuando no se cumple la ley de la conservación de la materia?
¿Cómo es que comprobar la ley de la conservación de la materia?
¿Dónde se aplica la ley de la conservacion de la masa?
¿Qué significa la ley de conservación de la masa y cómo es que se aplica en nuestra propia vida diaria?
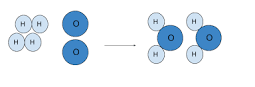
La ley de la conservación de la materia es la que mantiene que, dentro de un sistema cerrado, la cantidad total de materia que interviene en una sola reacción química es incesante. Comprendemos por sistema cerrado un entorno que aísla del exterior los militantes implicados en la reacción, como puede ser un recipiente sellado.
¿Quién dice que la materia no se crea ni se destroza?
¿Cómo se explica la ley de conservación de la masa?
Se puede enunciar de diferentes formas: La materia ni se está creando ni se destroza, sólo se transforma. En una sola reacción química la suma de la masa de los reactivos es igual a la suma de la masa de los productos.


















