¿Qué género de enlace es el CS2?
CS2: Apolar. La molécula posee dos links polares (C-S) dirigidos en la misma dirección y en sentidos opuestos, que se anulan entre sí.
¿Cómo es que se forma el CS2?
El sulfuro de carbono se obtiene por reacción directa de los elementos (vapor de agua de azufre y carbono) en ausencia de aire entre 800 y 1000 °C.
¿Cuál es la estructura de Lewis de CS?
En el modelo de Lewis, un sólo par de electrones compartido es un enlace fácil. Cada átomo de Cl interactúa con un total de ocho electrones de valencia: los seis en los pares solitarios y ambos dentro del enlace simple.
¿Cuántos electrones tiene el CS2?
¿Cuantos electrones se necesitan para ocupar el octeto del átomo central? No es correcto. El átomo de carbono comparte 4 electrones con los átomos de S. Eso supondría solo 6 electrones.
¿Qué tipo es el enlace tiene el compuesto disulfuro de carbono CS2?
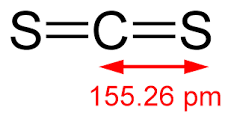
El disulfuro asimismo es utilizado para referirse a compuestos que poseen dos sulfuros. Por ejemplo, el disulfuro de carbono (Counter Strike 2 ), es una molécula con un centro de carbono y dos sulfuros unidos al átomo central por enlace doble: S=C=S.
¿Qué género de enlace es CO2 polar o apolar?
Polaridad de los enlaces covalentes
Izquierda: molécula de CO2. Si bien ambos enlaces CO son polares, la molécula, en grupo, es apolar, ya que el momento dipolar resultante es nulo.
Izquierda: molécula de CO2. Si bien ambos enlaces CO son polares, la molécula, en grupo, es apolar, ya que el momento dipolar resultante es nulo.
¿Qué tipo de enlace es c2?
La molecula de acetileno, C2H2, es el ejemplo más fácil de una molécula con enlace triple CC. Los compuestos que poseen este mismo enlace se llaman compuestos acetilénicos.
- ¿Qué tipo de enlace es Cl2 y por qué motivo?:
Dentro del Cl2 se unen dos átomos iguales con electronegatividades altas. Los dos tienen tendencia a ganar electrones para alcanzar la configuración de gas noble. Por eso se unirán compartiendo electrones. Se constituye un compuesto covalente.


















