¿Qué determina la orientación orbital en el espacio?
El valor de ml (número cuántico magnético) define la orientación espacial del orbital frente a un campo imantado externo.
¿Qué género de orbital está describiendo los números cuánticos?
Así, conseguimos los números cuánticos, n, l y m que definen absolutamente un orbital, mientras que los 4 números cuánticos n, l, m y s definen absolutamente un electrón que ocupa un orbital. Los números cuánticos son: 13 El número cuántico primordial, n, nos indica el nivel energético en el que nos hallamos.
¿Cómo es que se determina el número de orbitales?
Si n = 2, poseemos l = 0 (1 orbital 2s) y l = 1 (3 orbitales 2p). Si n = 3, tenemos l = 0 (1 orbital 3s), l = 1 (3 orbitales 3p) y l = 2 (5 orbitales 3d). Si n = 4, poseemos l = 0 (1 orbital 4s), l = 1 (3 orbitales 4p), l = 2 (5 orbitales 4d) y l = 3 (7 orbitales 4f).
¿Cuál es el número cuántico que indica el nivel de energía?
El número cuántico principal n escenifica la energía total relativa de cada orbital. El nivel de energía de cada orbital aumenta a medida que aumenta su separa del núcleo. Los conjuntos de orbitales con exactamente el mismo valor n a menudo se denominan capa de electrones.
¿Qué es un orbital de un átomo?
Un orbital atómico es la zona del espacio definido por una determinada solución particular, espacial e independiente del clima, a la ecuación de Schrödinger como para el caso de un electrón sometido a un potencial coulombiano.
¿Qué es un orbital atómico y molecular?
Así se llama a la combinación de los orbitales atómicos de dos átomos que están enlazados. Un orbital molecular se forma por un grupo de orbitales atómicos en un átomo de una molécula. La configuración electrónica de cada molécula depende de sus orbitales moleculares.
¿Quién definió el concepto de orbital atómico?
Con esta idea, Schrödinger llevó a cabo un estudio matemático del comportamiento del electrón en el átomo y obtuvo una expresion, conocida como ecuación de Schrödinger. Podemos proferir que un orbital atómico es una región del espacio adonde existe una alta probabilidad (muy superior al 90%) de encontrar al electrón.
¿Qué es un orbital en la tabla periódica?
Un orbital s es una esfera focalizada dentro del núcleo. Un orbital p, por la otra parte, tiene la forma de una pesa, con dos lóbulos definiendo adonde es probable que estén los electrones y un nodo en el medio que define la región adonde hay cero densidad de electrones. El núcleo se halla en éste nodo.
¿Qué es lo que significa orbital en química?
placeholder
¿Cuáles son los 4 géneros de orbitales?
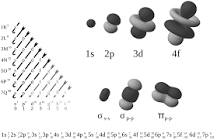
Indice
- 3.1 Orbitales s.
- 3.2 Orbitales p.
- 3.3 Orbitales d.
- 3.4 Orbitales f.
- 3.5 Orbitales g.
¿Cuál es la forma de los orbitales?
Así, todos y cada uno de los orbitales s tienen constituye esférica, mientras que los orbitales p, forma de dos lóbulos simétricos, solo se distinguen en la orientación dentro del espacio. – Orbitales tipo s: Todos y cada uno de los niveles de energéticos poseen este mismo tipo de orbitales.
¿En dónde se encuentra el orbital?
Un orbital es una zona del espacio alrededor del núcleo adonde existe una alta probabilidad de hallar electrones. El número máximo de electrones que puede haber dentro de un orbital es de dos. Los orbitales están pudiendo estar vacíos (sin electrones), repletos un 50% (1 electrón) o totalmente llenos.
¿Cuántos son los orbitales?
Así, hay 1 orbital tipo s, 3 orbitales p, 5 orbitales d y 7 del tipo f. De este mismo modo el número maximo de electrones que acepta cada subnivel es: 2 dentro del s; 6 en el p (2 electrones x 3 orbitales ); 10 dentro del d (2 x 5); 14 dentro del f (2 x 7).
¿Cuántos géneros de orbitales existen y cómo se representan?
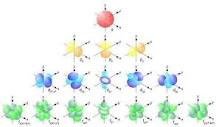
Existen cuatro tipos de orbitales los que son: s, p, d y f. Los orbitales son conocidos como subniveles de energía y cada uno de ellos puede contener el siguiente número de electrones: s= 2 electrones.
¿Cuántos tipos de orbitales moleculares hay y cuáles son?
Orbitales c3 * antienlazantes: Versión excitada (de mayor energía) de los enlazantes. Orbitales c0 * antienlazantes: Orbitales c0 de alta energía. Orbitales n: Para moléculas con heteroátomos (como el N o el O, verbigracia). Los electrones desapareados no participan dentro del link y ocupan este mismo orbital.
¿Qué es un orbital y que orbitales existen?
El orbital atómico es la zona y espacio energético que se halla al rededor del átomo, y en el como hay mayor probabilidad de hallar un electrón, el como realiza movimientos ondulatorios.


















