¿Cuál es la masa de SO3?
Masa molecular SO3 = 80.
¿Qué hay dentro de un mol de SO3?
– Calcula la masa molar del SO3 Solucion: La masa molar del SO3 se consigue de sumar la masa molar de 1 mol de átomos de azufre y la masa molar de 3 moles de átomos de oxígeno.
¿Cuántos átomos tiene el SO3?
Así, el símbolo SO3 representa la fórmula de la molécula constituída por tres átomos de oxígeno y uno de azufre, y asimismo indica la fórmula de la substancia pertinente, el trióxido de azufre.
- ¿Cuántos átomos tiene SO2?:
5.6.
La unidad elaborar de una sustancia molecular es la molécula; verbigracia, como para la sustancia dióxido de azufre, de fórmula SO2, la unidad elaborar es una molécula SO2, constituída por un átomo de azufre y dos de oxígeno, como su fórmula lo señala. - ¿Cuántos átomos tiene el SO2?:
Una molécula de dióxido de azufre, SO2, contiene un átomo de azufre y dos de oxígeno.
¿Cuánto es un mol de SO2?
Utilizando gramos: 1 mol de moléculas de SO2 (64,1 g) contiene 1 mol de átomos de azufre (32,1 g) y 2 moles de átomos de oxígeno (16,0 g).
- ¿Cuánto es un mol de h2s?:
Ácido sulfhídrico Propiedades físicas Apariencia gas incoloro Masa molar 34,1 g/mol Punto de fusión 187 K («1286 °C)
¿Cuál es el peso molecular de n2o3?
76,01 g/mol Óxido de nitrógeno / Masa molar
- ¿Cuál es el peso molecular de SO2?:
64,066 g/mol Dióxido de azufre / Masa molar
¿Cómo es que calcular la masa de SO2?
Utilizando unidades de masa atómica: Masa molecular del SO2 = (32,1) + (2 · 16) = 64,1 u.
¿Cómo calcular la masa de un ion?
Fórmula de masa de los compuestos iónicos
La fórmula de masa de un compuesto iónico se calcula de igual manera que la fórmula de masa de los compuestos covalentes: adicionando las masas atómicas promedio de todos los átomos de la fórmula del compuesto.
La fórmula de masa de un compuesto iónico se calcula de igual manera que la fórmula de masa de los compuestos covalentes: adicionando las masas atómicas promedio de todos los átomos de la fórmula del compuesto.
¿Cuántas moléculas hay en 1 mol de SO3?
Este número de teléfono nos señala que en cada mol de substancia hay un número total de 6.022×10²³ moléculas o átomos, fue planteado por Amedeo Avogadro.
¿Cómo es que calcular el peso molecular de SO3?
80,06 g/mol Óxido de azufre / Masa molar
¿Cuántos electrones tiene SO3?
En la molécula del SO 3, el átomo de azufre tiene un estado de oxidación de +6, con una está cargando formal de 0, y está rodeado de 6 pares de electrones.
¿Cómo formar el SO3?
‘4f El SO3 se forma cuando el anhídrido sulfuroso reacciona con agua en el aire. ‘4f El ácido sulfúrico se disuelve en agua dentro del aire y puede permanecer sobreseído dentro del aire por períodos de tiempo alterables.
¿Cuál es la estructura de Lewis del SO3?
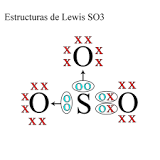
El azufre tendría 12 electrones en su ultima capa, 4 electrones mas sobre ocho (Ley del octeto) ésto se resuelve mediante dos sujeciones dativas (en las uniones dativas los electrones compartidos provienen de la remata castra de uno de sus átomos).
¿Cuánto es un mol de azufre?
Un mol de azufre tiene 6.022×10 23 átomos y su masa es de 32 gramos. Como para conocer la masa de un sólo átomo de azufre dividimos 1 mol a caballo entre 6.022×10 23 y ello lo multiplicamos por 32.


















