¿Qué es la constante Ebulloscopica y que indica?
Incesante ebulloscópia Una constante directa del descenso de la presión de vapor de un disolvente, por un soluto no volátil, es que la temperatura de ebullición de la disolución es bastante más alta que la del disolvente puro.
¿Cómo se calcula la constante Ebulloscopica?
«06T = Ke m «06T Ascenso ebulloscópico (ºC ó K). Ke Constante ebulloscópica (K·kg·mol-1). m Molalidad del soluto (mol·kg-1). «06T = Kc m «06T Descenso crioscópico (ºC ó K).
¿Qué significa que la constante Ebulloscópica del agua sea de 0 52 ºC mol kg?
Para el agua, el valor de la constante de ebullición es 0, 52 ºC / mol / Kg. Ésto quiere decir que una disolución molal de cualquier soluto en agua presenta una elevación ebulloscópica de 0, 52 º C.
¿Qué valor tiene la constante de ebullición?
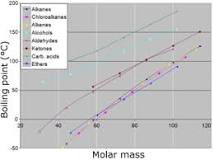
Existen dos convenciones respecto al punto de ebullición standard del agua: el punto de ebullición normal es 99.97 °C (211.9 °F) a una presión de 1 atm (o sea, 101.325 kPa).
¿Cuál es la constante Ebulloscópica del agua?
KE la constante ebulloscópica (en el agua es 0,512 ºC·kg/mol ) m la molalidad.
¿Qué influye dentro del aumento ebulloscópico?
En el ascenso ebulloscópico influye la cantidad total de partículas de soluto Disueltas en la disolución. Mientras más soluble sea el soluto, más partículas va a haber en la disolución y mayor sera el incremento ebulloscópico.
¿Cuánto vale la constante Ebulloscopica?
Siendo ‘4TE el incremento experimentado en la temperatura de ebullición = T-Te T:temperatura ebullición disolución Te:temperatura ebullición disolvente puro. KE la constante ebulloscópica (dentro del agua es 0,512 ºC·kg/mol ) m la molalidad.
¿Cómo se calcula el punto de ebullición?
¿Cómo se calcula el punto de ebullición? T 1 es la temperatura de ebullición ( punto de ebullición ) del militante, mesura a la presión de 1 bar (P 1 ) y expresada en ºc Kelvin (K). P 2 es la presión de vapor de agua del militante expresada en bar o bien en atm.
¿Cuáles son las formulas de las propiedades coligativas?
es el número de moles de soluto. Se utiliza de manera frecuente para determinar masa molar del soluto (M2) disuelto, para ello m se expresa como: m = w2 1000 / w1 M2 (5) w1 gramos de solvente, w2 gramos de soluto.
¿Cómo se calcula el descenso crioscópico?
5.5 Para solutos electrolitos y disociables la ecuación para el descenso crioscópico se escribe así: T = i Kf m.
Estas mismas propiedades entre otros usos se usan como para:
Estas mismas propiedades entre otros usos se usan como para:
- Minoración en la temperatura de congelación.
- Aumento de la temperatura de ebullición.
- Disminución de la presión de vapor.
¿Qué dice la ley de Raoult?
La ley de Raoult consiente calcular la presión de vapor de agua de una substancia en cuanto está constituyendo parte de una disolución idónea, conociendo su presión de vapor en cuanto está mera (a exactamente la misma temperatura) y la composición de la disolución idónea en concepto de fracción molar.
¿Que son y cuáles son las propiedades coligativas del agua?
Existen cuatro propiedades coligativas: el descenso crioscópico, el ascenso ebulloscópico, la presión osmótica y el descenso de la presión de vapor.
¿Cómo calcular la constante de ebullición?
¿Cómo se calcula el punto de ebullición? T 1 es la temperatura de ebullición (punto de ebullición ) del componente, medida a la presión de 1 bar (P 1 ) y expresada en grados Kelvin (K). P 2 es la presión de vapor del militante expresada en bar o en atm.
¿Qué valores tienen la temperatura de fusion y la de ebullición?
| Substancia | Punto de Fusión Normal (K) | Puntode Ebullición Normal (K) |
|---|---|---|
| Mercurio | 234 | 630 |
| Agua | 273.15 | 373.15 |
| Azufre | 392 | 717.75 |
| Plomo | 600.5 | 2023 |
¿Qué punto de ebullición?
Es la temperatura a la que se produce el cambio de la fase líquida a la fase gaseosa. A esa temperatura la presión de vapor de agua de un líquido es una atmosfera. Dentro del Sistema Internacional se mide en K (Kelvin).


















