¿Qué aporto François Marie Raoult a la fisicoquimica?

En 1887, expresó la fluctuación de la presión de vapor de agua, al mostrar que la minoración relativa de la presión de vapor (a la misma temperatura), de un líquido volátil al disolver en él un soluto no salino cualquiera, es igual a la fracción molar del soluto, que se conoce como la ley de Raoult.
¿Quién descubrio la ley de Raoult?
¿Qué dice la ley de Raoult?
¿Qué género de soluciones obedecen la ley de Raoult?
¿Quién inventó el soluto?
¿En cuanto no se cumple la ley de Raoult?
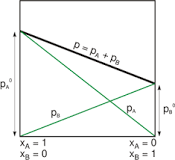
Las desviaciones negativas de la ley de Raoult emergen en cuanto las fuerzas entre las partículas en la mezcla son más fuertes que la media de las fuerzas a caballo entre las partículas en los líquidos puros.
¿Cuándo se suma un soluto no volátil a un solucione volátil la presión de vapor de agua de la solucion resultante con correlación a la presión de vapor del solucione puro es?
¿Qué estipula la ley de Raoult y la ley de Henry?
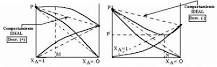
A una T cte, la cantidad de gas disuelta dentro de un líquido es de forma directa proporcional a la presión parcial que ejercita ese gas acerca de el líquido.’ El gas con mayor presión parcial en una sola mezcla tendrá mayor masa en la solucion. Mayor presión que ejerce un gas, mayor número de teléfono de choques que hay a caballo entre las moléculas.
- ¿Qué estipula la ley de Raoult PDF?:
La ley de Raoult establece que la relación a caballo entre la presión de vapor de cada militante en una solución ideal depende de la presión de vapor de cada militante puro y de su fracción molar en la solución.
¿Qué propone la ley de Raoult respecto a las propiedades coligativas?
¿Qué apps tiene la ley de Raoult ejemplos?
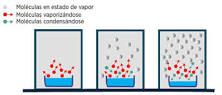
Una de las apps de la ley de Raoult es la separación de los compuestos puros presentes en una sola disolución a través de la técnica de instilación, en la cual los militantes son separados por diferencia de temperatura.
¿Qué solucion obedece la ley de Raoult?
¿Qué mezclas binarias presentan un comportamiento idónea?
¿Cuándo es apropiado utilizar la ley de Raoult modificada?

La principal aplicación que se le da a la Ley de Raoult es la destilación, ya sean destilaciones sencillas (distintos puntos de ebullición) como para separar militantes puros o destilaciones fraccionadas (puntos de ebullición próximos a caballo entre sí).


















