¿Cuál fue el experimento que realizó Rutherford?
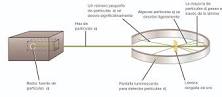
El experimento de la lámina de oro de Rutherford mostró que los átomos son mayoritariamente espacio vacío, junto con un pequeño y denso núcleo de forma positiva cargado. Basado en éstos desenlaces, Rutherford propuso el modelo nuclear del átomo.
¿Cuáles fueron las conclusiones del experimento de Rutherford?
Puesto que sólo unas pocas partículas fueron con fuerza dispersadas (repelidas) por los átomos de oro, Rutherford arribó a la conclusión de que los átomos deben tener una parte en la cual se concentra la está cargando positiva. Denominó a ésta parte el núcleo.
¿Cómo explicar la teoria de Rutherford?
El Modelo de Rutherford establecía: El átomo tiene un núcleo central en el cual estan concentradas la carga positiva y prácticamente toda la masa. La está cargando positiva de los protones es compensada con la está cargando negativa de los electrones, que se hallan fuera del núcleo.
¿Cómo fue la experimento de Rutherford?
Los ensayos que diseñaron implicaron bombardear una lámina metálica con partículas alfa para observar cómo la lámina los desperdigó en correlación con su espesor y material. Utilizaron una pantalla fluorescente como para medir las trayectorias de las partículas.
¿Qué experimento hicieron Rutherford y Geiger?
Ernest Rutherford y sus propios estudiantes Geiger y Marsden dealizaron un experimento vital para el desarrollo de la Física Atómica. Investigaron la penetración y dispersión de partículas alfa a través de una fina lámina de oro.
¿Qué aportacion esencial realizó el experimento de e Rutherford?
Su Aportación a la Ciencia
En 1902, con la cooperación de Henri y Soddy, Rutherford postuló la teoría sobre la radioactividad natural y descu- brieron las partículas radiactivas (alpha, beta y gamma).
En 1902, con la cooperación de Henri y Soddy, Rutherford postuló la teoría sobre la radioactividad natural y descu- brieron las partículas radiactivas (alpha, beta y gamma).
¿Qué hechos consiguió explicar el modelo atómico de Rutherford?
– El modelo atómico de Rutherford
Con sus ensayos pudo inferir que el átomo estaba constituido por una zona central positiva adonde se concentraba toda la masa y que los electrones giraban en órbitas al rededor del núcleo, como si fuese un pequeño sistema pavimentar.
Con sus ensayos pudo inferir que el átomo estaba constituido por una zona central positiva adonde se concentraba toda la masa y que los electrones giraban en órbitas al rededor del núcleo, como si fuese un pequeño sistema pavimentar.
¿Qué conclusion saco Rutherford?
Rutherford concluyó que el hecho de que la mayoría de las partículas atravesaran la hoja metálica, señala que una gran parte del átomo está vacío, que la desviación de las partículas alfa indica que el deflector y las partículas contienen está cargando positiva, pues entonces la desviación siempre es dispersa.
¿Que deseó revisar Rutherford con su experimento?
Los experimentos de Rutherford fueron una serie de televisión de ensayos históricos a través de los cuales los científicos descubrieron que cada átomo tiene un núcleo adonde tiene las estás cargando positivas y la mayor una parte de su masa se concentran.
¿Cuál es la relevancia del modelo de Rutherford?
La relevancia del modelo de Rutherford residió en plantear la existencia de un núcleo dentro del átomo. Concepto que, paradójicamente, no aparece en sus escritos. Lo que Rutherford consideró importante, como para explicar los resultados experimentales, fue ‘una concentración de carga’ dentro del centro del átomo.


















