¿Qué resuelve el modelo atómico de Bohr?
EL ÁTOMO DE BOHR
Adoptando el modelo de Rutherford, Bohr propuso como para el átomo de hidrógeno, un núcleo conformado por una partícula positiva, y virando en torno a ella, un electrón. Este mismo es el modelo planetario adonde el núcleo es el sol y los electrones los planetas.
Adoptando el modelo de Rutherford, Bohr propuso como para el átomo de hidrógeno, un núcleo conformado por una partícula positiva, y virando en torno a ella, un electrón. Este mismo es el modelo planetario adonde el núcleo es el sol y los electrones los planetas.
¿Qué problemas o dificultades dieran respuesta al modelo atómico de Bohr?
El modelo de Bohr no pudo explicar, de manera cuantitativa, ciertas de las divisiones observadas. 3. – Además de esto, el modelo no proporcionaba explicación alguna para el resplandor relativo (intensidad) de las líneas fantasmales.
¿Qué problemas superó el modelo atómico de Bohr y porqué?
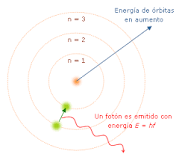
Como para superar este mismo dilema Bohr supuso que los electrones nada más se podían mover en órbitas concretas, cada una de las cuales caracterizada por su nivel energético. Cada órbita puede entonces identificarse mediante un número de teléfono entero n que toma evalúes a partir de 1 en adelante.
¿Cuáles son los alcances del modelo atómico de Bohr?
Bohr procuraba hacer un modelo atómico capaz de explicar la estabilidad de la asignatura y los espectros de emisión y succión discretos que se vigilan en los gases. Describió el átomo de hidrógeno con un protón dentro del núcleo, y virando a su al rededor un electrón.
¿Cuáles son los alcances y limitaciones del modelo de Bohr?
Hola Isabel, El modelo de Bohr es restringido en concepto de las predicciones en átomos con muchísimos electrones: Primero, se obtienen predicciones espectrales deficientes cuando se trata de átomos con Z grandes. Segundo, no puede pronosticar las intensidades relativas de las lineas espectrales.
¿Qué logro explicar el modelo atómico de Bohr?
Bohr describió el átomo fundamental del hidrógeno como un electrón moviéndose en orbitas circulares cerca de un protón, representando este último al núcleo del átomo, el cual Bohr sitúa en su parte central y dando una explicación recia respecto de la estabilidad de la órbita del electrón y del átomo en su conjunto
- ¿Que no pudo explicar el modelo atómico de Bohr?:
No obstante el modelo atómico de Bohr también debió ser abandonado al no poder explicar los fantasmas de átomos más complejos. La idea de que los electrones se mueven alrededor del núcleo en órbitas definidas debió ser desechada.
¿Cuáles son las limitaciones del modelo atómico?
La primordial limitación de Rutherford fue afirmar que los electrones de los átomos constituían órbitas. No están pudiendo ser consideradas órbitas pues no se puede saber el movimiento y la trayectoria de un electrón. Sólo probabilidades. Un electron constituye orbitales, nubes de electrones.
¿Cuál es la relevancia del modelo de Bohr?
El modelo de Bohr fue el primero en reconocer el concepto de la mecanica cuántica en la estructura electrónica de un átomo de hidrógeno y, además, develó cómo era la estabilidad de los átomos.
¿Cómo es que se aplica el modelo de Bohr?
Bohr propone un modelo en el cual los electrones sólo pueden ocupar ciertas órbitas circulares. Los electrones se organizan en capas y, en todos y cada castra tendrán una cierta energía, llenando siempre las capas inferiores (de menor de edad energía) y después las superiores.
¿Cómo es que resuelve Bohr los problemas que presentaba el modelo atómico de Rutherford?
Respuesta: Fue propuesto en 1913 por el físico danés Niels Bohr, para explicar cómo los electrones están pudiendo poseer órbitas estables al rededor del núcleo y por qué los átomos presentaban fantasmas de emisión característicos (dos problemas que eran ignorados dentro del modelo anterior de Rutherford).
¿Cuál fue el error del modelo de Rutherford?
El principal dilema del modelo de Rutherford fue que aceptó que los electrones viraban en órbitas circulares en compresor al núcleo, según ésto los electrones se deberían desplazar a gran velocidad, lo cual así como la órbita que describen los haría perder energía colapsando con el núcleo. Hoy se sabe que ésto no está sucediendo.
¿Qué impacto tuvo el modelo atómico de Bohr?
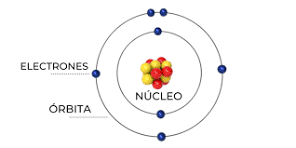
Bohr entrañó que los electrones se movían en órbitas circulares al rededor del núcleo. Niels Bohr desarrolló su modelo de consenso a tres postulados fundamentales: Los electrones están describiendo órbitas circulares en compresor al núcleo del átomo sin irradiar energía.


















