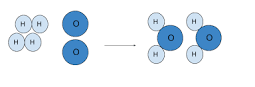
¿Cómo es que se aplica la ley de la conservación de la materia en una sola ecuación química?
¿Cómo es que se comprueba la ley de la conservación de la materia en los balanceos de ecuaciones químicas?
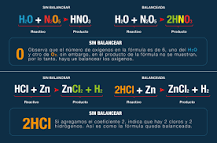
Al balancear las reacciones químicas buscamos que se cumpla la Ley de la conservación de la materia. El procedimiento de tanteo para mecer una ecuación química consiste en igualar el número y clase de átomos, iones o moléculas reactantes con los productos a fin de cumplir la Ley de la conservación de la materia.
¿Cómo se evidencia la ley de la conservación de la materia?
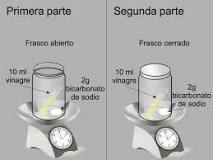
- ¿Cómo se evidencia la ley de la conservación de la materia en una reacción química de bicarbonato de sodio con vinagre?:
Al entrar en contacto el vinagre y el bicarbonato se produce una reacción química con desprendimiento de dióxido de carbono gaseoso. Y al acrecentar la presión dentro del interior del recipiente se infla el zepelín en cuestión de segundos.
- ¿Cómo se manifiesta la ley de la conservación de la materia?:
Ejemplo 1: Combustión de una vela
En cuanto una vela arde no se gana ni se está perdiendo masa. La masa total de la cera y del oxígeno molecular (O bien 2 ) presente antes de la combustión es igual a la masa total de dióxido de carbono (CO 2 ), vapor de agua (H 2 O) y cera sin abrasar que quedan en cuanto la candela se apaga.
¿Qué significa que la materia ni se crea ni se destruye solo se transforma?

principio de consevación de la masa o bien ley de Lavoisier.
La materia ni se crea ni se destruye, solo se transforma. En una sola reacción química la suma de la masa de los reactivos es igual a la suma de la masa de los productos. En una sola reacción química los átomos no desaparecen, simplemente se ordenan de otro modo.
¿Qué nos afirma la ley de la conservación de la materia?
¿Quién afirmó que la energía ni se crea ni se destruye solo se transforma?
La energía no se crea ni se destruye, solo se transforma , o bien, como dijo Antoine Lavoisier (imagen a la derecha), padre de la química moderna, ya dentro del siglo XVIII: La materia ni se crea ni se destruye, sólo se transforma (lo que en el fondo es exactamente lo mismo).
- ¿Qué ley dice que la energía nose crea ni se destruye solo se transforma?:
La ley de la conservación de la energía estipula que la energía no puede crearse ni destruirse, sólo transformarse de una forma de energía a otra. Esto significa que un sistema siempre tiene exactamente la misma cantidad de energía, salvo que se añada a partir de el exterior.
¿Qué creador afirmó que la materia no se crea ni se destruye solo se transforma dentro del trascurso de los fenómenos?
¿Qué es la ley de Lavoisier ejemplos?
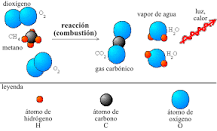
Ejemplos en reacciones químicas
En cuanto una candela arde no se gana ni se está perdiendo masa. La masa número total de la cera y del oxígeno molecular (O 2 ) presente antes de la combustión es igualito a la masa total de dióxido de carbono (CO 2 ), vapor de agua (H 2 O bien) y cera sin quemar que quedan en cuanto la vela se apaga.
¿Quién dice que la materia no se crea ni se destruye?
¿Cómo se aplica la ley de Lavoisier en la vida cotidiana?
- La descomposición de la fruta. Es notable la reducción del tamaño del comestible a medida que se degrada.
- Fundir hielo. Al dejar un vasito con hielo a temperatura ambiente el hielo se funde.
- Hervir agua.
- Objetos oxidados.
- Capacitación de compuestos.
¿Cómo es que demostró su ley Lavoisier?
¿En cuanto no se cumple la ley de Lavoisier?
¿Cómo es que tiene por nombre la ley de conservación de la materia?
¿Cómo lleva por nombre la ley de Lavoisier?
Se puede enunciar de diferentes formas: La materia ni se crea ni se destruye, solo se transforma. En una sola reacción química la suma de la masa de los reactivos es igualito a la suma de la masa de los productos.
¿Qué es la ley de la conservación de la masa ejemplos?
¿Qué teoria contradice la ley de la conservacion de la materia?
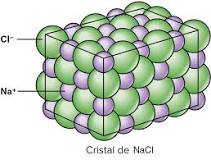
La teoría atómica de Dalton.
¿Qué estipula la ley Estequiométrica?
Por lo cual su ley afirma: la materia no se crea ni se destruye, solo se transforma. 2. – Ley de las proporciones constantes Esta ley es también conocida como ley de las proporciones definidas o fijas.
¿Cuáles son las 5 leyes ponderales?
- 1.1 Ley de Lavoisier o bien de conservación de la masa.
- 1.2 Ley de Proust o bien de las proporciones constantes.
- 1.3 Ley de Dalton o bien de las proporciones múltiples.
- 1.4 Ley de Richter o de las proporciones análogos o recíprocas.
- 1.5 Ley de Gay-Lussac o de los volúmenes de combinación.
¿Cómo se descubrio la ley de conservacion dela materia?
Hallazgo de la ley de conservación de la materia
Fue el científico ruso Mikhail Lomonosov (1711-1765 ) quien probó por vez primera la conservación de la materia en 1756. Lo hizo al mostrar cómo unas placas de plomo no cambiaban de peso mientras tanto se quemaban dentro de un recipiente sellado (sin contacto con el aire).
- ¿Cómo es que se creó la ley de conservacion de la materia?:
La ley de la conservación de la materia se desarrolla en el siglo XVIII merced a dos científicos, Mijaíl Lomonósov y Antoine Lavoisier, que de manera paralela, alcanzaron conclusiones afines. Abundantes hechos de nuestro día a día prueban lo cual mantiene este principio básico de la química.
¿Qué nos dice la ley de Lavoisier?
¿Qué estipula la ley dela conservación dela materia?
¿Qué llevó a cabo Lavoisier en 1785?

En junio de 1783, Lavoisier realizó reaccionar oxígeno con aire inflamable, obteniendo ‘agua en estado muy puro’. Finalizó debidamente que el agua no era un elemento, sino más bien un compuesto de oxígeno y aire inflamable (o bien hidrógeno, como se conoce ahora).
- ¿Qué llevó a cabo Lavoisier en 1774?:
Lavoisier demostró en 1774 que el aire es una mezcla de oxígeno y otro gas, ázoe.
¿Cómo es que se reveló la ley de la conservación de la masa?
¿Que utilizo Lavoisier para sus propios cálculos químicos?
¿Cómo es que puede aplicarse el principio de conservación de la masa a los cambios químicos?
¿Qué aportación de Lavoisier le dejó demostrar su ley explica su experimento?
La suma número total de los pesos, ya antes y despues del experimento, era la misma. De ésta forma, Lavoisier probó que la materia no se crea ni se destruye.
¿En dónde se puede aplicar la ley de conservación de la masa materia?
¿Quién demostró y enunció la ley de conservación que afirma que la materia no se crea ni se destruye solo se transforma?
¿Cuándo y quién enuncio la ley de la conservación de la materia por qué se le califica de un revolucionario?
¿Quién descubrió la ley de la conservación de la materia?
¿Qué dice la ley de la conservación de la materia ejemplos?
- ¿Qué dice la ley de conservacion dela materia ejemplos?:
Dice que dentro de un sistema aislado, a lo largometraje de cualquier proceso judicial físico o químico, la masa se mantiene constante. Esto quiere decir que durante los procesos físicos o bien químicos la materia no se crea ni se destruye, simplemente, se transforma.