¿Cuál es la diferencia entre la energía y el calor?
- ¿Cuál es la diferencia entre temperatura calor y energía?:
El calor se puede asimilar a la energía número total del movimiento molecular en una sustancia, mientras tanto temperatura es una medida de la energía molecular intermedia. El calor depende de la velocidad de las partículas, su número, su tamaño y su tipo. La temperatura no depende del tamaño, ni del número o del tipo.
- ¿Cuál es la diferencia entre calor y energía Brainly?:
Contestación: Calor es la temperatura ya sea alta o bajita y energía es el resultado última del trabajo efectuado.
¿Que entiende por energía interna energía térmica y calor?
¿Qué relación hay entre el calor y la energía?
- ¿Qué relación existe entre el calor y la energía cinética?:
Una mayor temperatura involucra una mayor energía cinética de las moléculas, por lo que va a aumentar la probabilidad de que las choques sean productivas.
- ¿Qué diferencia hay entre el calor y la energía?:
La energía térmica de un cuerpo depende del grado de agitación de las partículas que lo componen. La energía de cada partícula puede ser muy diferente, pero el valor medio de comunicación de ésta energía se corresponde con la temperatura que marcan los termómetros. El calor es la constituye en que se está ganando o se pierde energía térmica.
¿Qué relación existe entre el calor y la energía interna de una sustancia?
¿Cuál es la diferencia entre calor y trabajo?
¿Qué es la energía térmica o bien calor?
¿Cómo se relacionan entre si el calor la energía interna y la energía térmica?
Todos los cuerpos poseen energía interna, tenido que en parte a la energía cinética de sus propios partículas. Esta energía se llama energía térmica. A mayor velocidad de las partículas mayor es la energía del cuerpo. La temperatura es una magnitud macroscópica.
¿Qué relacion existe entre calor y energía interna?
¿Cuál es la relacion que existe entre el calor y la temperatura?

El calor se puede asimilar a la energía número total del movimiento molecular en una sustancia, mientras tanto temperatura es una mesura de la energía molecular intermedia. El calor depende de la rapidez de las partículas, su número, su tamaño y su tipo. La temperatura no depende del tamaño, ni del número o del género de partículas.
¿Cómo se correlaciona la energía interna con el calor y el trabajo?
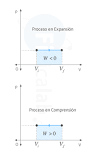
La primera ley de la termodinámica estipula una relación entre la energía interna del sistema y la energía que intercambia con el entorno en constituye de calor o trabajo. Está considerada positivo aquello que aumenta la energía interna del sistema, o bien lo que es lo mismo, el trabajo recibido o el calor absorbido.
¿Qué relación existe entre el calor suministrado a un sistema y la energía interna y el trabajo externo realizado por el sistema?
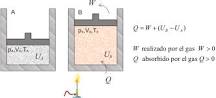
Un sistema termodinámico puede canjear energía con su enclave en constituye de trabajo y de calor, y amontona energía en forma de energía interna. La relación entre estas tres magnitudes viene impartida por el comienzo de conservación de la energía.



















